吉林大學/華南理工大學Biomaterials:仿生聯合組裝納米藥物用于抑制化療導致的乳腺癌轉移
發布時間:2021-02-24 09:50:40 人氣:1866
化療是治療乳腺癌患者的主要方法之一。但矛盾的是,它往往也會導致癌癥的進一步發展和轉移。了解化療后轉移機制有助于開發新的治療策略以改善化療導致的癌癥發展。在這項研究中,吉林大學陳立教授、張明副教授、華南理工大學邵丹研究員和楊超博士在阿霉素(Dox)處理的4T1乳腺癌細胞中對HMGB1在TLR4介導的上皮至間質轉化(EMT)過程中的調控作用進行了研究。
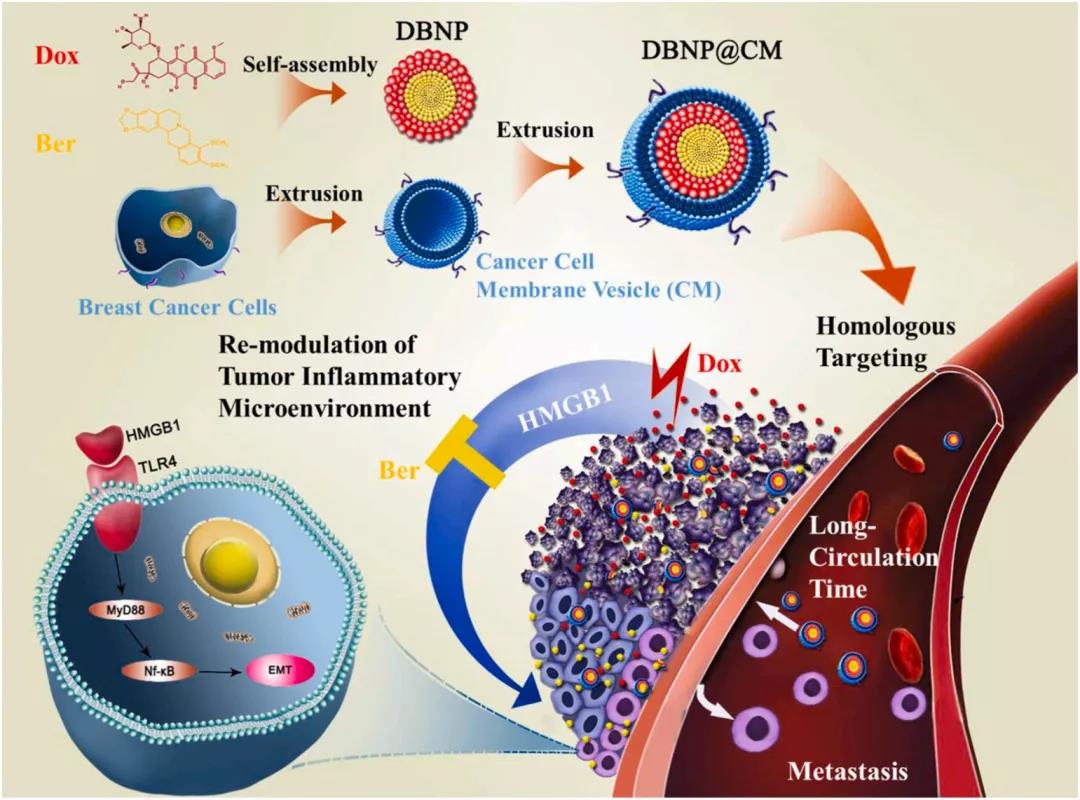
本文要點:
(1)小檗堿(Ber)是一種經臨床批準的生物堿,已被證明是一種HMGB1-TLR4調節劑,會在體內外促進乳腺癌的轉移。首先,實驗假設聯合使用Dox和Ber對于乳腺癌的化療有益,并設計了由Dox和Ber組成的自組裝納米藥物(DBNP)。
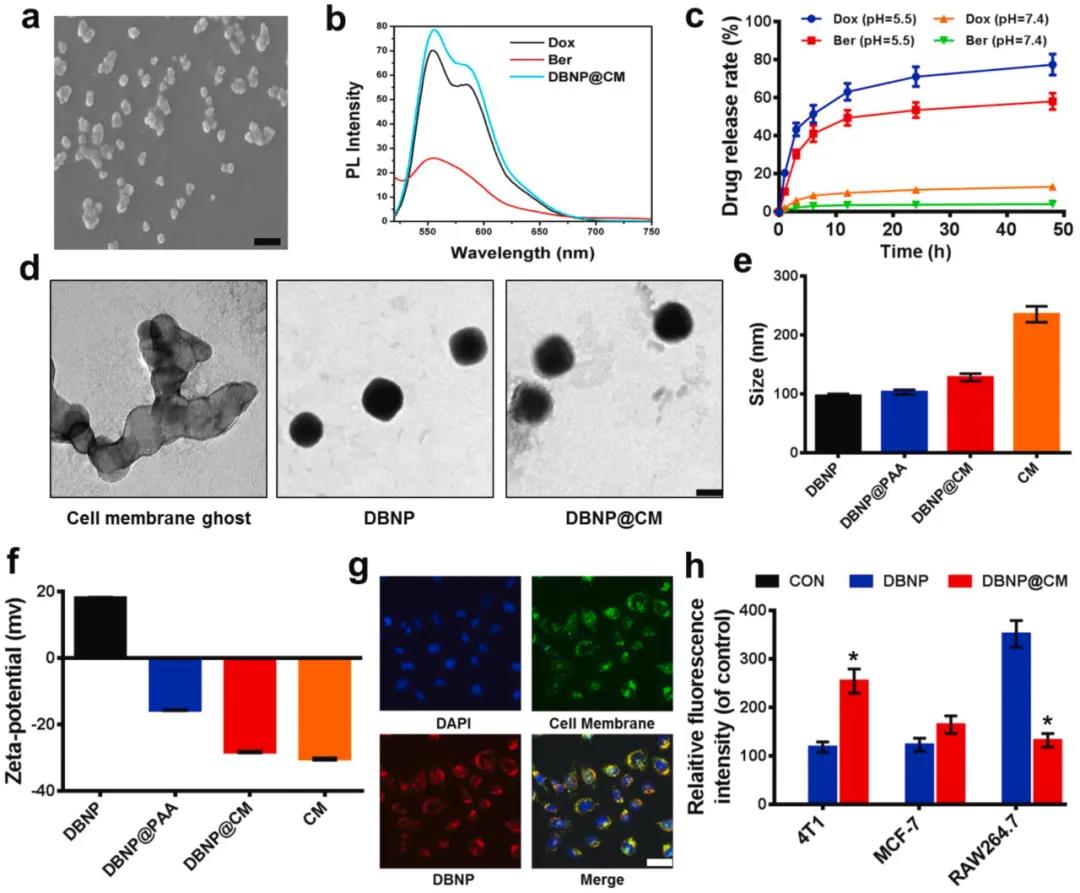
(2)在4T1荷瘤小鼠中,經4T1細胞膜(CM)包裹后的DBNP@CM在腫瘤部位的積累量明顯高于DBNP,且血液循環時間更長。研究表明,DBNP@CM不僅能有效抑制腫瘤生長,副作用更低,并且可通過阻斷HMGB1-TLR4以顯著抑制腫瘤的肺轉移。綜上所述,這一研究結果為抑制化療導致的乳腺癌轉移提供了一個聯合策略,并為開發有效、安全的乳腺癌化療仿生納米藥物提供了新的途徑。
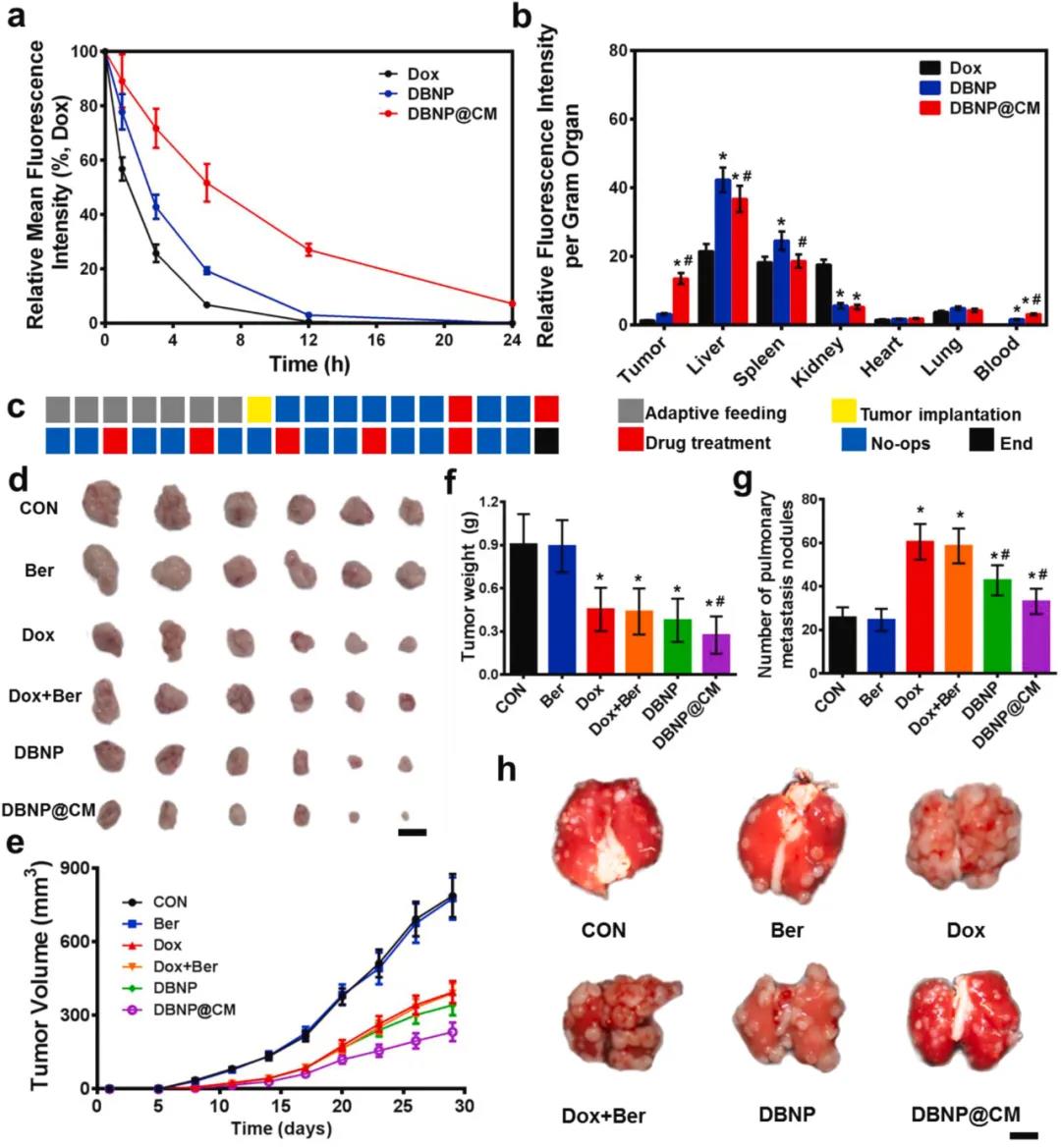
參考文獻
Xiao Zheng. et al. Biomimetic co-assembled nanodrug of doxorubicin and berberine suppresses chemotherapy-exacerbated breast cancer metastasis. Biomaterials. 2021
https://www.sciencedirect.com/science/article/pii/S0142961221000673
| 溫馨提示:蘇州北科納米供應產品僅用于科研,不能用于人體,不同批次產品規格性能有差異。網站部分文獻案例圖片源自互聯網,圖片僅供參考,請以實物為主,如有侵權請聯系我們立即刪除。 |
下一篇: 納米醫學產品1


